 臺北醫學大學幹細胞醫學研究又有新突破,成功解開胚胎生殖系幹細胞在類似胚胎發育極度缺氧情況下,如何進行幹細胞對稱性分裂與細胞遷移之分子機制,為未來的癌症治療找到新契機。
臺北醫學大學幹細胞醫學研究又有新突破,成功解開胚胎生殖系幹細胞在類似胚胎發育極度缺氧情況下,如何進行幹細胞對稱性分裂與細胞遷移之分子機制,為未來的癌症治療找到新契機。
本校細胞治療與再生醫學研究中心主任黃彥華特聘教授指出,藉由這項突破性研究成果,可進一步推演固體腫瘤癌幹細胞如何在沒有氧氣的環境中,進行癌幹細胞對稱性分裂及癌轉移,致使病人產生抗藥性與早期復發的機制,未來可望透過癌症轉譯醫學,開發癌症治療標靶癌幹細胞的新方法,研究論文已於2018年2月發表於幹細胞國際權威學術期刊《幹細胞報告》(Stem Cell Reports)。
 北醫大校友、義大醫院院長杜元坤教授為了鼓勵母校在幹細胞醫學研究領域持續精進,在2018年3月21日的記者會上慷慨解囊,每年將捐資200萬元,連續10年,總計2千萬元,做為母校細胞治療基礎轉譯研究、臨床試驗及高階人才培育的發展基金,期能拋磚引玉,將臺北醫學大學打造為全球細胞治療與再生醫學重鎮,嘉惠更多患者。【右圖:杜元坤院長(右)慨捐2千萬元給母校作為細胞治療基礎轉譯研究相關基金,由林建煌校長(左)代表接受】【下左圖:黃彥華主任簡報幹細胞研究突破狀況】
北醫大校友、義大醫院院長杜元坤教授為了鼓勵母校在幹細胞醫學研究領域持續精進,在2018年3月21日的記者會上慷慨解囊,每年將捐資200萬元,連續10年,總計2千萬元,做為母校細胞治療基礎轉譯研究、臨床試驗及高階人才培育的發展基金,期能拋磚引玉,將臺北醫學大學打造為全球細胞治療與再生醫學重鎮,嘉惠更多患者。【右圖:杜元坤院長(右)慨捐2千萬元給母校作為細胞治療基礎轉譯研究相關基金,由林建煌校長(左)代表接受】【下左圖:黃彥華主任簡報幹細胞研究突破狀況】
 黃彥華主任表示,精子及卵子結合受孕後,在胚胎發育最早期會產生胚胎幹細胞,由於當時完全沒有血管,胚胎幹細胞就在無氧環境中快速增生及爬行。幹細胞的增生機制包括「非對稱性分裂」與「對稱性分裂」;在有氧氣的情況下,組織細胞進行非對稱性分裂,每次只產生一個幹細胞,其他為分化細胞,藉以形成具功能性的體組織;在早期胚胎極低氧氣的環境下,胚胎期幹細胞則進行對稱性分裂,每次可產生兩個完全相同具高能力的幹細胞,因此可迅速地大量累積胚胎期幹細胞的數量。【左圖:黃彥華主任】
黃彥華主任表示,精子及卵子結合受孕後,在胚胎發育最早期會產生胚胎幹細胞,由於當時完全沒有血管,胚胎幹細胞就在無氧環境中快速增生及爬行。幹細胞的增生機制包括「非對稱性分裂」與「對稱性分裂」;在有氧氣的情況下,組織細胞進行非對稱性分裂,每次只產生一個幹細胞,其他為分化細胞,藉以形成具功能性的體組織;在早期胚胎極低氧氣的環境下,胚胎期幹細胞則進行對稱性分裂,每次可產生兩個完全相同具高能力的幹細胞,因此可迅速地大量累積胚胎期幹細胞的數量。【左圖:黃彥華主任】
而癌幹細胞是一群細胞數極少、處休眠期、且具高抗藥性與癌症轉移能力的細胞,它不需要氧氣就能存活,一般能生存於後期較大固體腫瘤內部深處缺氧的惡劣環境,一旦患者的免疫力下降,或出現發炎反應或病毒感染,就會伺機而動。黃主任指出,癌幹細胞的抗藥性與轉移令醫生束手無策,若遇上缺氧環境即會壯大勢力使之更難應付,這也是導致許多癌症患者早期復發,並產生抗藥性導致治療無效的重要元凶,癌症細胞狡猾兇狠的程度,一如《哈利波特》系列電影中的「佛地魔」,令人望而生畏。
 截至目前為止,醫學界尚不清楚調控癌幹細胞增生的分子機制,無法針對癌幹細胞進行標靶治療,就算治療後腫瘤變小,癌幹細胞還是繼續殘留在腫瘤中,伺機而動。
截至目前為止,醫學界尚不清楚調控癌幹細胞增生的分子機制,無法針對癌幹細胞進行標靶治療,就算治療後腫瘤變小,癌幹細胞還是繼續殘留在腫瘤中,伺機而動。
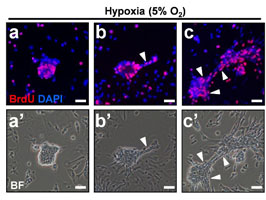
此時,癌幹細胞往往會聰明地學習胚胎幹細胞在低氧環境下的增生機制,充分利用固體腫瘤在低氧環境中容易促使細胞對稱性分裂的特性,快速增生而導致腫瘤早期復發,既殺不死又生生不息,且有很強的細胞遷移作用,會隨著時間開疆闢土、造成癌版圖擴張,我們卻無可奈何。【右圖:早期胚胎缺氧微環境下,胚胎期幹細胞增生與轉移情形】

 為徹底解決這個棘手問題,北醫大在林建煌校長帶領下,領先亞洲整合學校以及附屬醫院的細胞治療與再生醫學等資源,先後成立「細胞治療與再生醫學研究中心、GTP核心實驗室與細胞治療與再生醫學國際博士學位學程」,將全身安全性的細胞治療產品列為開發計畫,從基礎研究、轉譯醫學、法規倫理、轉譯產學到生醫新創衍生公司,聚焦醫療未滿足疾病轉譯研究與產業發展,同時配合政府推動細胞治療與再生醫學發展政策,全力提升學術研究能量,培育臨床醫療研究人才,為未來推動細胞臨床醫療貢獻心力。【上圖:林建煌校長(左圖)與杜元坤院長(右圖)致辭】
為徹底解決這個棘手問題,北醫大在林建煌校長帶領下,領先亞洲整合學校以及附屬醫院的細胞治療與再生醫學等資源,先後成立「細胞治療與再生醫學研究中心、GTP核心實驗室與細胞治療與再生醫學國際博士學位學程」,將全身安全性的細胞治療產品列為開發計畫,從基礎研究、轉譯醫學、法規倫理、轉譯產學到生醫新創衍生公司,聚焦醫療未滿足疾病轉譯研究與產業發展,同時配合政府推動細胞治療與再生醫學發展政策,全力提升學術研究能量,培育臨床醫療研究人才,為未來推動細胞臨床醫療貢獻心力。【上圖:林建煌校長(左圖)與杜元坤院長(右圖)致辭】
黃彥華主任指出,研究中心以解決醫療未滿足的醫療問題為標的,聚焦於組織再生、胸腔醫學、癌症治療、神經疾病之基礎轉譯研究、臨床試驗推行與全身安全性細胞治療商品開發,近年來研究成果卓著。
這項研究未來可利用於固體腫瘤包括腦瘤、肝癌、肺癌、胰臟癌、大腸直腸癌等,癌幹細胞都可能利用類似的機制,在體內不斷自我更新快速增生,並且往外竄逃,再隨著血液循環轉移至全身各處,無時無刻都在找尋下一個落腳處。
本篇論文第一作者郭勇哲博士後研究員表示,胚胎生殖系幹細胞基礎研究是以胚胎鼠與新出生小鼠為來源,在實驗室純化取得胚胎期幹細胞後,隨即進行有氧與缺氧環境初代培養,並在極有限的細胞數量下重複進行悉數實驗,以不到3年時間完成所有欲了解的關鍵環節,技術領先全球。
北醫大研究團隊藉由了解胚胎期幹細胞的調控訊息傳遞,藉此推演在固體癌組織中癌幹細胞的快速增生與轉移機制。研究團隊將進一步進行轉譯醫學研究,利用缺氧與其衍生的相關訊息,設計藥物及治療方法,期望能為癌症病患重新找回健康人生。(文/細胞治療與再生醫學研究中心‧秘書處)【下圖:林建煌校長(左4)率李飛鵬副校長(右2)、吳介信副校長(左3)、公共事務處蘇維文處長(左2)、黃彥華主任(右1)、崔岡特別助理(左1)等與杜元坤院長(右3)合影】


